尿路上皮癌是泌尿系统常见的恶性肿瘤之一,90%的尿路上皮癌发生于膀胱[1]。人表皮生长因子受体2(HER-2)在尿路上皮癌的发生发展中起重要作用,但是单纯HER-2单抗类药物和抗HER-2酪氨酸激酶抑制剂在转移性HER-2过表达尿路上皮癌中并未显示出显著的临床疗效,而研究显示抗HER-2抗体偶联药物(ADC)能够给HER-2过表达(IHC 2+和3+)局部晚期或转移性尿路上皮癌患者带来显著临床获益[1],进一步研究发现其联合免疫检查点抑制剂可以大幅提高有效率[2]。山东省立医院宁豪教授分享1例HER-2过表达特殊变异亚型尿路上⽪癌合并“冰冻盆腔”病例,患者经ADC联合PD-1单抗新辅助治疗后顺利完成手术,术后病理示由术前cT4b降期为ypT1。术后采用ADC药物联合PD-1单抗维持治疗半年。目前患者总生存期(OS)已经超过16个月。【肿瘤资讯】将病例诊疗过程整理如下,并特邀山东省立医院吕家驹教授对病例进行点评,以飨读者。
病例介绍
患者63岁男性,既往体健,吸烟史40余年。
患者于2022年2月底无诱因出现“尿频、尿急、尿痛”膀胱刺激症状,症状进行性加重,抗炎治疗无效;患者快速出现“下腹部疼痛不适、腹肌僵硬”症状,夜尿增加至30余次。2022年3月8日患者就诊于当地医院,泌尿系超声提示:膀胱充盈⽋佳,膀胱壁厚、⽑糙。CTU示:双肾输尿管(-),膀胱充盈⽋佳,前壁增厚,最厚处约3cm,边缘⽑糙,周围脂肪间隙模糊(图1)。盆腔MR示:膀胱充盈⽋佳,壁明显增厚,最厚处约2.7cm,边缘⽑糙,周围间隙模糊,盆腔内及下腹部周围软组织肿胀(图2)。膀胱镜检查示:膀胱挛缩容量缩⼩,膀胱右前壁增厚,粘膜滤泡样隆起。活检病理示:低度恶性潜能未定尿路上⽪肿瘤,局部上⽪增⽣活跃。
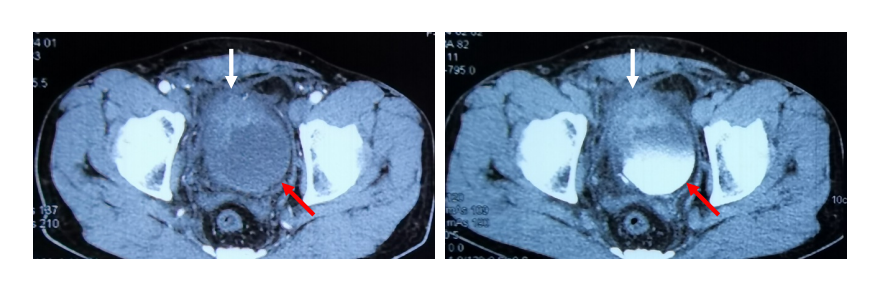
图1 2022年3月外院CT
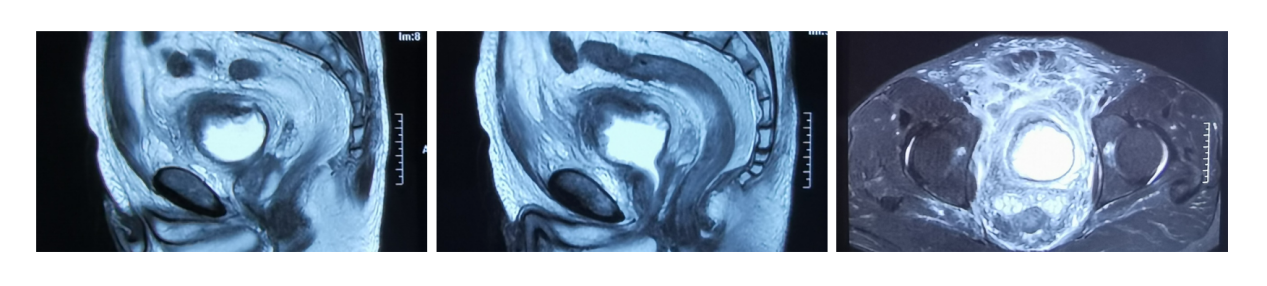
图2 2022年3月外院MR
2022年3月17日患者转入我院,尿脱落细胞学检查示:查⻅可疑癌细胞。患者下腹僵硬似“板状腹”,疾病进展迅速,血肌酐(Cr)快速升高,因尿量减少,尿频症状得以缓解。
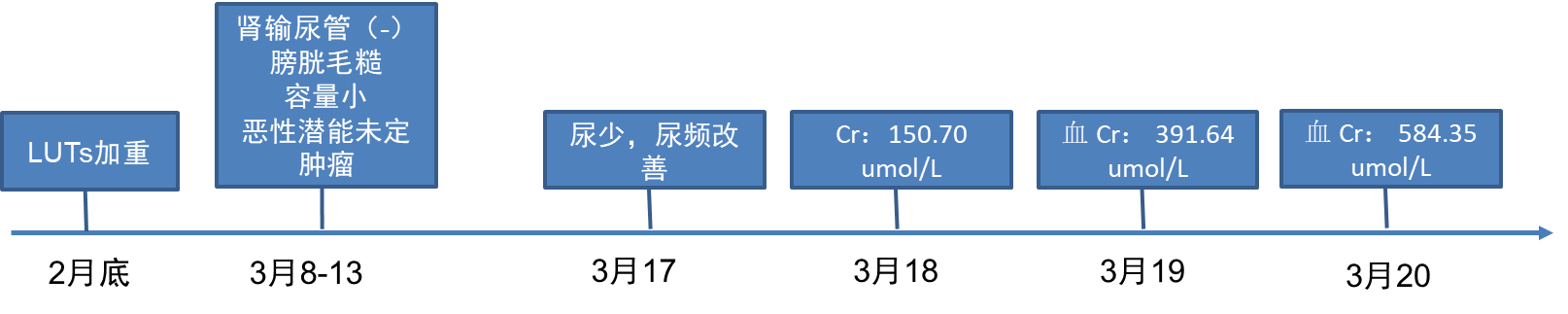
2022年3月20日晨Cr:584.35 umol/L↑,拟膀胱镜下置双J管。膀胱镜下见:膀胱容量<40ml,膀胱粘膜增厚,均呈滤泡样隆起改变,双侧输尿管⼝未能窥及,⽆法置管(图3),遂超声引导下行双肾穿刺造瘘置管引流。2022年3月21日晨复查血 Cr将至179.46 umol/L↑。
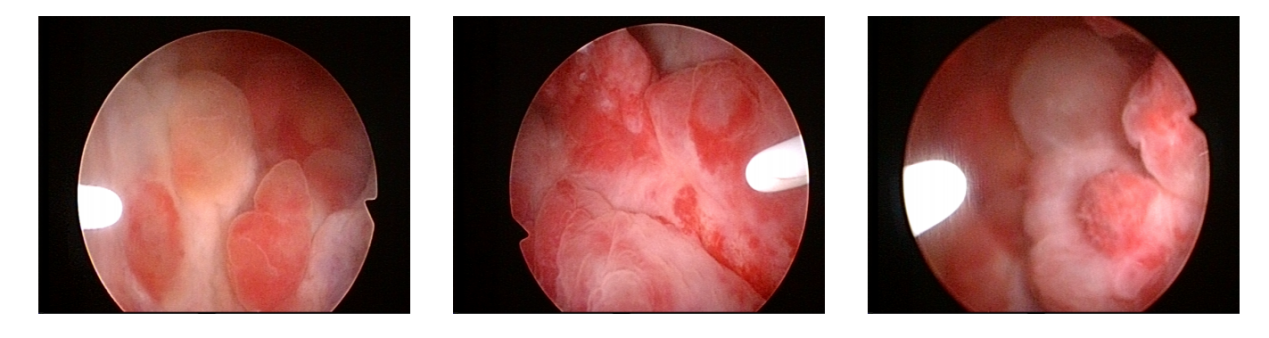
图3 2022年3月本院膀胱镜
2022年3月21日于全麻下拟行腹腔镜下膀胱全切+尿流改道术。⼿术中情况: 在全麻多次追加肌松情况下,下腹壁仍坚硬如石;气腹压升高至20mmHg下腹及盆腔空间仍狭小;整个下腹前壁及盆腔呈“冰冻”⻣盆改变(图4)。决定旷置膀胱,仅⾏双侧输尿管⽪肤造⼝,然后改截⽯位⾏诊断性电切。2022年3月25日电切病理示:(膀胱肿瘤)浸润性尿路上⽪癌,⾼级别(淋巴瘤样和浆细胞样变异型),脉管内查⻅癌。免疫组化示:GATA-3(+),P40(+),P63(+),HER-2(2+), CK(AE1/AE3)(+)。PD-L1(22C3)阳性综合评分CPS< 1,阴性。
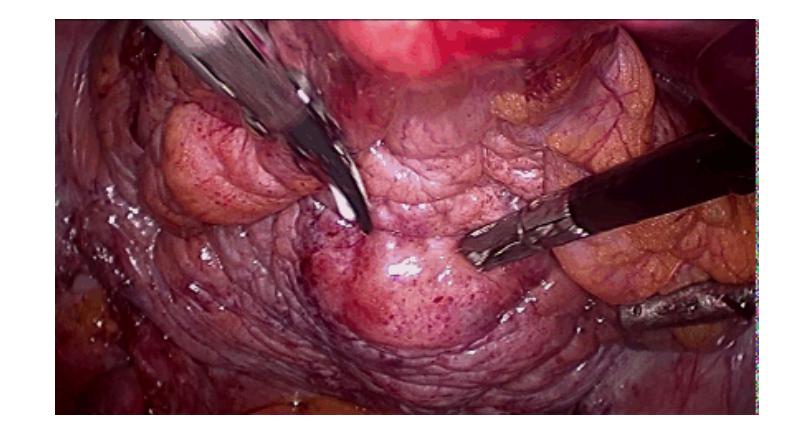
图4 2022年3月⼿术中情况:无法辨认脐动脉、输精管等解剖标志
患者目前分期考虑为:cT4bN0M0。2022年3月31日我院泌尿肿瘤MDT团队对该病例进行了充分讨论:①考虑疾病进展迅速,应尽快启动全身系统治疗;②患者刚经历了急性肾衰,化疗耐受性差;③根据文献报道的浆细胞样变异型尿路上皮癌的免疫微环境及HER2的表达特点,结合该患者HER-2(2+)表达情况,认为抗HER-2ADC药物联合PD-1单抗是潜在的有效选择。遂于2022年4月1日开始替雷利珠单抗每三周一次 + 维迪⻄妥单抗每两周一次的系统治疗。治疗过程中,患者耐受性良好,无SAE发生;每月复查全腹部及盆腔CT提示:膀胱周围间隙逐渐改善;腹壁⽔肿逐渐改善;同时患者腹壁僵硬及下腹疼痛症状也逐渐消失。
在经历了维迪⻄妥单抗7个周期+替雷利珠单抗6个周期治疗后,患者查体示:下腹平软,僵硬“板状腹”表现已完全消失。2022年7月15日复查盆腔MR与2022年3月盆腔MR片相比,膀胱周围间隙显著改善,盆腔内及下腹部周围软组织肿胀显著改善(图5)。患者疗效评价:临床部分缓解(cPR)或临床完全缓解(cCR)状态。经院内及院际MDT讨论后于2022年7月28日再⾏腹腔镜下膀胱全切术(图6),顺利将病变膀胱切除(图7)。术后病理示:由术前cT4b降期为ypT1(图8)。
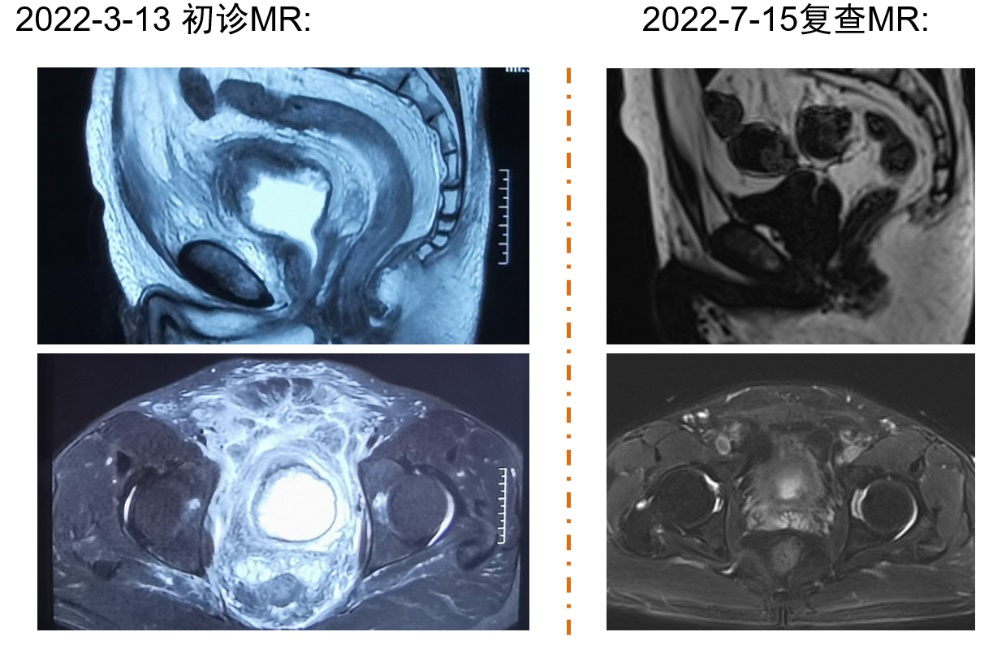
图5 治疗前和治疗后MR对比
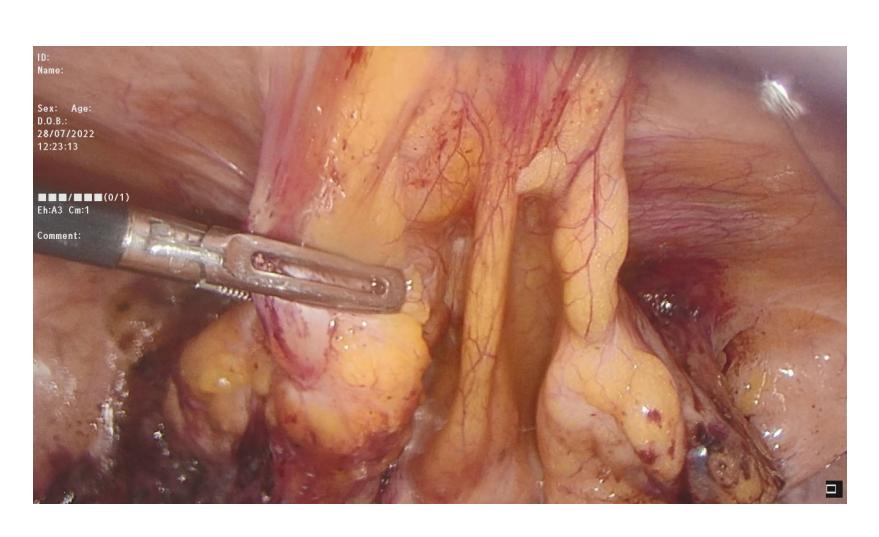
图6 2022年7月⼿术中情况:可辨认脐动脉、输精管等解剖标志
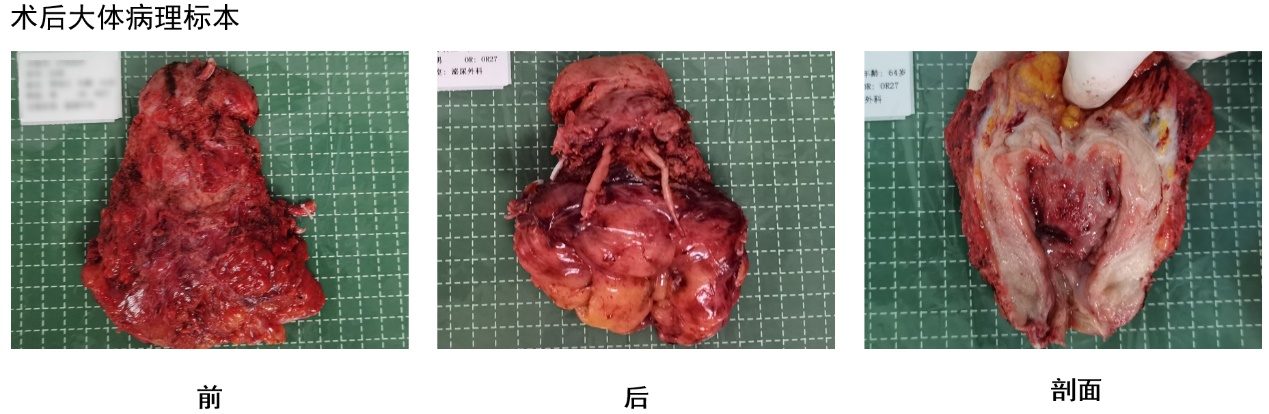
图7 大体病理标本
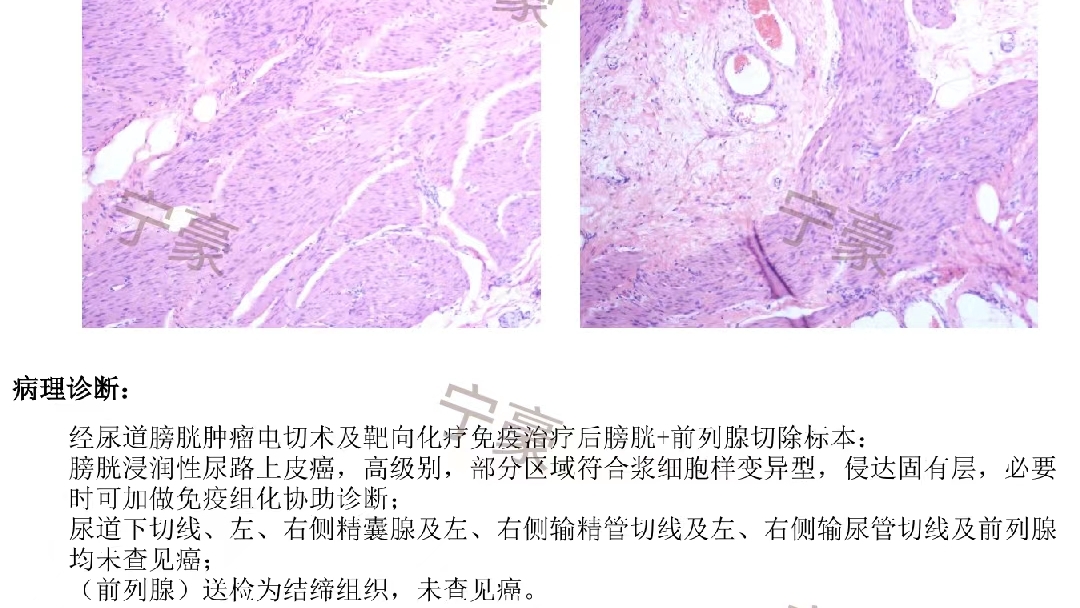
图8 术后病理结果
经再次院际及院内MDT讨论,决定予以患者术后半年的维持治疗。患者于2022年8月29日开始接受替雷利珠单抗+维迪⻄妥单抗每三周一次的维持治疗。患者⽬前已结束维持治疗半年,持续影像学随访无复发。
病例点评
该患者是一例cT4bN0M0的浸润性浆细胞样尿路上⽪癌患者,HER-2表达阳性(2+),PD-L1表达阴性。患者第一次手术因“冰冻盆腔”无法实施膀胱全切,采用维迪西妥单抗联合PD-1单抗新辅助治疗七个周期后成功实现降期,顺利完成腹腔镜下膀胱全切术,术后采用ADC药物联合PD-1单抗维持治疗半年。维迪西妥单抗联合PD-1单抗围手术期治疗取得了突出疗效,目前患者无复发生存(RFS)已经超过12个月,还在持续随访中。
以顺铂为基础的化疗方案是肌层浸润性膀胱尿路上皮癌的标准新辅助治疗方案[3],但是含铂化疗毒副作用大,据报道新辅助化疗在肌层浸润性膀胱癌患者中的总体应用率不到20%[4],亟需寻找更加安全高效的围手术期治疗方案。维迪西妥单抗是我国自主研发的抗HER-2ADC药物,在探索其联合PD-1单抗用于局部晚期或转移性尿路上皮癌患者的安全性和活性的RC48-C014研究[2]中,所有患者确认的客观缓解率(ORR)为73.2%,完全缓解(CR)率为9.8%,疾病控制率(DCR)为90.2%,中位无进展生存期(PFS)为9.2个月,2年OS率为63.2%。亚组分析显示,维迪西妥单抗联合PD-1单抗一线治疗的ORR达到76.0%;HER-2 IHC 3+/2+、IHC 1+和IHC 0人群的ORR分别为83.3%、64.3%和33.3%。且联合治疗的安全性可控。该研究结果表明,维迪西妥单抗联合PD-1单抗能够给HER-2过表达的尿路上皮癌患者带来临床获益,不受PD-L1表达限制,且HER-2低表达及阴性患者也能从联合治疗中获益。基于RC48-C014研究结果,《中国临床肿瘤学会(CSCO)尿路上皮癌诊疗指南(2023)》[5]将维迪西妥单抗联合PD-1单抗纳入一线治疗推荐,并推荐所有局部晚期或转移性尿路上皮癌患者进行常规HER-2检测。
RC48-C017研究[6]是一项开放、单臂、II期多中心临床研究,旨在评价维迪西妥单抗联合PD-1单抗在肌层浸润性膀胱癌围手术期治疗中的疗效和安全性,研究计划入组40例既往未接受过系统治疗的cT2-T4aN0-1M0期肌层浸润性膀胱癌患者,研究者确认的HER-2表达为IHC 3+/2+、1+。在新辅助治疗阶段,使用维迪西妥单抗联合PD-1单抗治疗6周期(Q2W),随后进行膀胱癌根治性手术。完成了膀胱根治性术后,继续进行辅助治疗,直至疾病进展,或者出现患者无法耐受的不良反应为止。主要研究终点为病理完全缓解(pCR)率,次要终点为病理缓解率(yp≤T1N0)、ORR、1年无病生存(DFS)率、OS、不良反应等。目前研究正在进行中,期待能够取得突破,为广大尿路上皮癌患者提供更优的围手术期治疗策略。
参考文献
[1] 中国抗癌协会肿瘤病理专业委员会, 中国临床肿瘤学会尿路上皮癌专家委员会. 中国尿路上皮癌人表皮生长因子受体2检测临床病理专家共识[J]. 中华肿瘤杂志, 2021, 43(10):1001-1006.
[2] Sheng XN, et al. 2023 ASCO, Abstract 4566.
[3] 中华人民共和国国家卫生健康委员会. 膀胱癌诊疗指南(2022年版).
[4] 赵罡健,沈冲,吴周亮等.免疫检查点抑制剂在肌层浸润性膀胱癌新辅助免疫治疗中的研究进展[J].现代泌尿外科杂志,2022,27(08):700-706.
[5] 中国临床肿瘤学会(CSCO)尿路上皮癌诊疗指南(2023).
[6] ClinicalTrials.gov Identifier: NCT05297552.
来源:肿瘤咨询
