泰它西普
作用机制
泰它西普是我们专有用于治疗自身免疫性疾病的新型融合蛋白,由人跨膜激活剂及钙调亲环素配体相互作用因子(TACI)受体的胞外域以及人免疫球蛋白G(IgG)的可结晶片段(Fc)域构成。泰它西普靶向两类对B淋巴细胞发育至关重要的细胞信号分子:B淋巴细胞刺激因子(BLyS)和增殖诱导配体(APRIL),得以有效降低B细胞介导的自身免疫应答,自身免疫应答与多种自身免疫性疾病有关。
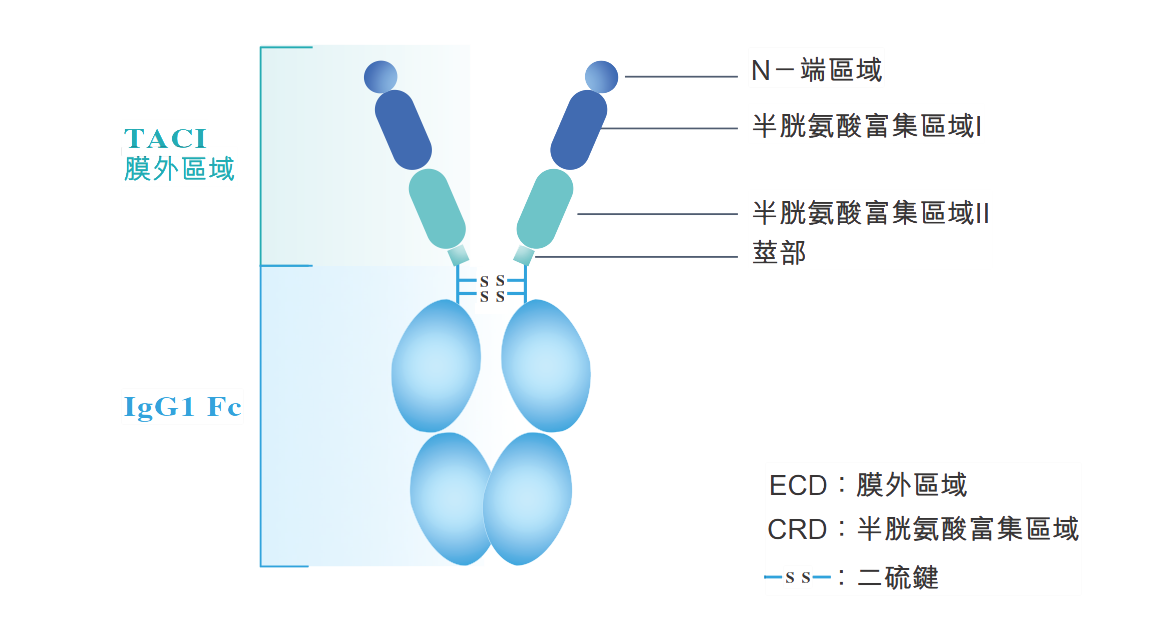
BLyS(又称B细胞活化因子或BAFF)和APRIL均参与B细胞从前B淋巴细胞发育为成熟的B细胞,最终发育成为专职产生抗体的浆细胞,并在若干条件下共同刺激T细胞增殖。已知B细胞异常的活化和抗体产生与许多自身免疫性疾病有关。BLyS和APRIL通过以下机制发挥功能:
• BLyS结合B细胞上表达的三类膜受体,即TACI、B细胞成熟抗原(BCMA)及B细胞活化因子受体(BAFF-R),以抑制细胞死亡并刺激B细胞分化为产生抗体的浆细胞。BLyS和TACI之间的相互作用诱导独立于T细胞的B细胞活化、免疫球蛋白类别转换和B细胞内稳态,而BLyS与BCMA的相互作用对于浆细胞的分化和存活非常重要。
• 与BLyS不同,APRIL仅与TACI和BCMA(而非BAFF-R)结合以调节B细胞的功能和存活,并促进其分化为浆细胞。
• 总而言之,BCMA与BLyS的结合较弱,而BAFF-R不与APRIL结合,TACI以相等的亲和力与BLyS和APRIL结合,也可以与BLyS和APRIL的异聚形式结合。
• BLyS和APRIL在联合刺激T细胞及B细胞与T细胞互相干扰方面也发挥了作用。例如,由于BAFF-R是潜在的T细胞协同刺激因素,BLyS向BAFF-R发出的信号可能促进异常的T细胞成熟,这被认为与若干自体免疫性疾病存在关连。
与已知功能一致,在SLE、NMOSD、RA等B细胞介导自身免疫性疾病中观察到BLyS和APRIL表达增加。研究表明对BLyS和APRIL的直接抑制有可能阻止其受体BAFF-R、TACI和BCMA的参与,从而阻止其后激活B细胞驱动机制,如产生自身抗体引发自身免疫性疾病病状。因此,BLyS和APRIL已成为自身免疫治疗的重要靶点,尽管针对该信号通路的大部分临床阶段候选药物旨在中和BLyS或APRIL而非同时中和两者。
如下图所示,泰它西普阻止BLyS和APRIL与B细胞表面表达的BAFF-R、BCMA及TACI受体结合,抑制BLyS及APRIL信号传导,并抑制成熟B细胞和浆细胞的发育和存活。
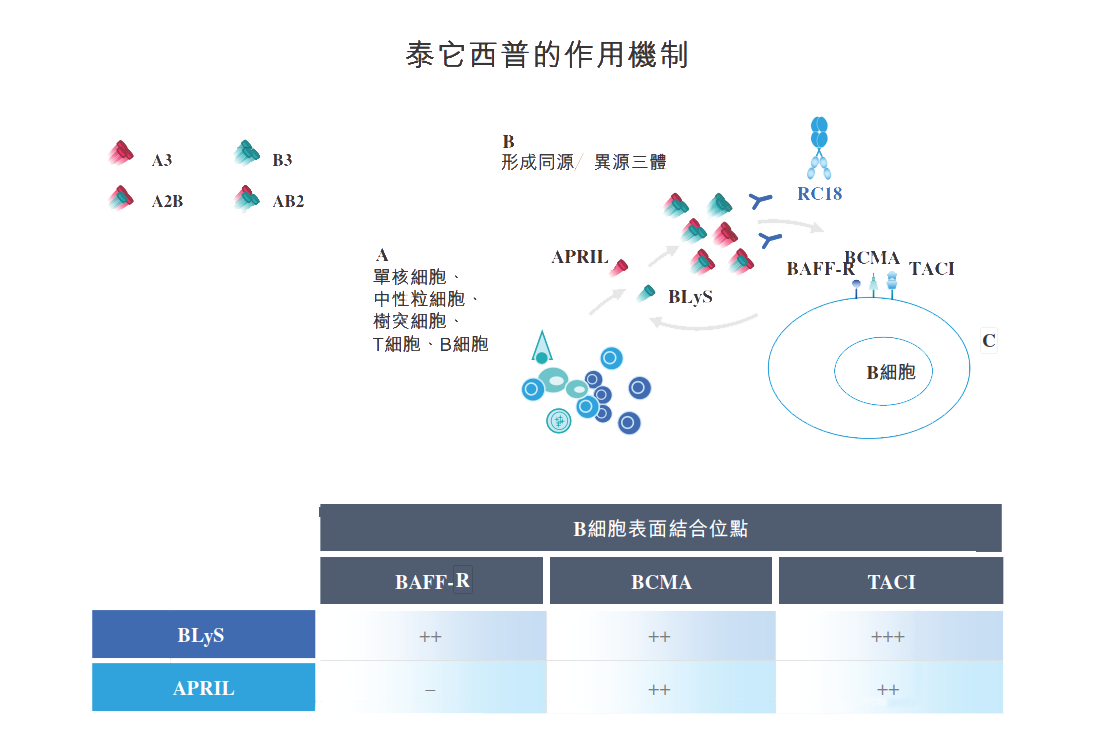
缩略语:A3 = APRIL同源三聚体;B3 = BLyS同源三聚体;A2B = 两种APRIL及一种BLyS分子的异源三聚体;AB2 = 一种APRIL及两种BLyS分子的异源三聚体。
适应症
泰它西普是全球首款治疗系统性红斑狼疮(SLE)的双靶生物新药。2021年3月,泰它西普治疗系统性红斑狼疮的新药上市申请经优先审评审批程序,作为具有突出临床价值的临床急需药品在中国获附条件批准上市,并于同年底进入国家医保药品目录;2023年11月,泰它西普正式获得国家药品监督管理局同意,由附条件批准转为完全批准。2024年7月,其类风湿关节炎适应症获批上市;2024年10月,重症肌无力适应症上市申请获CDE受理,并被纳入优先审评审批程序。
除系统性红斑狼疮以外,我们正在积极开展泰它西普用于治疗视神经脊髓炎谱系疾病、IgA肾病、原发性干燥综合症、和全身型重症肌无力等多种B细胞介导的、临床需求未被充分满足的难治性自身免疫性疾病的临床研究。

竞争优势
• 结构设计优势
-独特的双靶点机制提高阻断效果 -较好的生物活性 -较好的稳定性和延长的半衰期 -优化的免疫耐受性 -较低的免疫原性
• 生产优势
人源化以及经过分子信息学优化之后的分子结构设计有效提高了泰它西普的分子稳定性,延长了半衰期,更加适用于大规模工业化生产。目前,我们已建设了符合GMP要求的融合蛋白生产设施,已实现融合蛋白产品的稳定和高效生产,可以满足注册性临床以及商业化后的生产需求。
• 临床前及临床疗效优势
基于泰它西普独特的双靶点设计和经生物信息学优化的蛋白结构,泰它西普在临床前及临床试验中展示了良好的疗效及安全性,且在临床试验中未观察到药物相关的免疫原性。